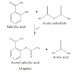
Sintesis aspirin diklasifikasikan sebagai reaksi esterifikasi. Asam salisilat diolah dengan asetat anhidrida, turunan asam, menyebabkan reaksi kimia yang mengubah gugus hidroksil asam salisilat menjadi gugus ester (R-OH → R-OCOCH3). Proses ini menghasilkan aspirin dan asam asetat, yang dianggap sebagai produk sampingan dari reaksi ini. Sejumlah kecil asam sulfat (dan terkadang asam fosfat) hampir selalu digunakan sebagai katalis.
Awalnya terinspirasi oleh sakit artritis yang diderita ayahnya, yaitu Hoffmann seorang berkebangsaan Jerman mensintesis suatu senyawa bernama asam asetilsalisilat (aspirin). Dengan senyawa ini Hoffmann dapat mengobati ayahnya tanpa mengakibatkan iritasi perut yang parah seperti efek samping pada obat artritis pada masa itu. Aspirin atau asam asetilsalisilat (asetosal) merupakan suatu jenis obat dari keluarga salisilat yang sering digunakan sebagai analgesik (terhadap rasa sakit atau nyeri minor), antipiretik (terhadap demam), dan anti-inflamasi. Aspirin ini juga memiliki efek antikoagulan dan digunakan dalam dosis rendah dalam tempo lama untuk mencegah serangan jantung.
Aspirin dibuat dengan mereaksikan asam salisilat dengan anhidrida asam asetat dengan menggunakan katalis 85% H3PO4 sebagai zat penghidrasi atau juga dapat direaksikan dengan asam asetat glacial bila asam asetat anhidrad sulit untuk ditemukan.. Asam salisilat merupakan asam bifungsional yang mengandung dua gugus –OH dan –COOH. Karenanya asam salisilat ini dapat mengalami dua jenis reaksi yang berbeda yaitu reaksi asam dan reaksi basa. Suatu reaksi dengan anhidrida asam asetat akan menghasilkan aspirin. Kemurnian aspirin tersebut bisa diuiji dengan menggunakan besi(III) klorida. Besi (III) klorida bereaksi dengan gugus fenol akan membentuk kompleks ungu. Asam salisilat (murni) akan berubah menjadi ungu jika ditambahkan FeCl3, karena asam salisilat mempunyai gugus fenol. Selain itu, kemurnian aspirin juga dapat ditentukan dengan uji titik leleh, dimana seharusnya titik leleh aspirin murni adalah 136oC.
Reaksi Sintesis Aspirin

Dengan mekanisme seperti dibawah ini,

Fungsi dari 85% H3PO4 yang ditambahkan yaitu sebagai katalis dalam reaksi sintesis asam asetilsalisilat dan pemberi suasana asam karena reaksi berlangsung pada suasana asam. Penggunaan asam fosfat dapat digantikan dengan asam sulfat. Reagen lain yang dapat digunakan dalam sintesis aspirin ini yaitu anhidrida asam asetat. Anhidrida asam asetat yang digunakan karena hasil esterifikasi fenol akan mendapatkan hasil yang lebih baik apabila digunakan derivat asam karboksilat yang lebih reaktif. Anhidrida asam asetat adalah derivat yang lebih reaktif yang dapat menghasilkan ester asetat. Reaksi tersebut juga dilakukan pada air yang dipanaskan agar mempercepat tercapainya energi aktivasi. Sedangkan pendinginan dimaksudkan untuk membentuk kristal, karena ketika suhu itu dingin, molekul-molekul aspirin dalam larutan akan bergerak melambat dan pada akhirnya terkumpul membentuk endapan melalui proses nukleasi (induced nucleation) dan pertumbuhan partikel. Mekanisme reaksi yang terjadi yaitu sebagai berikut :
- Anhidrida asetat menyerang H+.
- Anhidrida asam asetat mengalami resonansi.
- Anhidrida asam asetat menyerang gugus fenol dari asam salisilat.
- H+ terlepas dari –OH dan berikatan dengan atom O pada anhidrida asam asetat.
- Anhidrida asam asetat terputus menjadi asam asetat dan asam asetilsalisilat.
PERMASALAHAN
- Aspirin ini dibuat dengan cara esterifikasi, dimana bahan aktif dari aspirin yaitu asam salisitat direaksikan dengan asam asetat anhidrad atau dapat juga direaksikan dengan asam asetat glacial bila asam asetat anhidrad sulit untuk ditemukan. Mengapa asam asetat anhidrad ini dapat digantikan dengan asam asetat glacial? Apakah karna memiliki sifat yang sama? Jelaskan! (Vika Seputri)
- Aspirin merupakan suatu ester dari asam asetat dengan asam salisilat. Aspirin dapat dibuat dengan mereaksikan asam salisilat dengan anhidrida asam asetat menggunakan asam fosfat pekat sebagai katalisator. Bagaiman jika yang di gunakan sebagai katalisator berupa asam pekat lain? misalnya asam sulfat pekat. (Nadiya)
- Dikatakan bahwasannya sintesis aspirin diperoleh dari stating material yaitu asam asetat anhidrid yang direaksikan dengan asam salisilat diamana keduanya merupakan senyawa karboksilat Dan digunakan H2SO4 sebagai katalisnya yang dilakukan secara pemanasan dengan suhu 50-60derajat agar bisa menghasilkan senyawa asetil salisilat (aspirin) Nah bagaimana jika suhu yg digunakan lebih dari 60 misalnya saja 70 derajat apakah aspirin masih dapat terbentuk? (Nurhalimah)
- Secara teoritis, jumlah aspirin yang dihasilkan adalah setara dengan jumlah asam salisilat yang direaksikan. Apakah yang dapat membuat hal ini terjadi dan bagaimana cara memperbanyak produk aspirin tanpa menambah jumlah asam salisilat? (Kelantan)
- Permasalahan :reaktan berlebih yang seperti apa yang bisa menggeser kesetimbangan ke kanan untuk mendukung pembentukan aspirin ? (Nur khalishah)
- Dikatakan bahwa dibanding asam salisilat asam asetil salisilat merupakan asam yang lebih lemah. Pada pelarutan dengan penambahan basa akan terjadi hidrolisis yang cepat atau lambat menjadi salisilat dan asetat tanpa bergantung pada konsentrasi ion OH. Selain itu, dalam suasana asam juga akan terhidrolisis. Mengapa demikian? (Wisliana)



Tidak ada komentar:
Posting Komentar